20(S)-ginsenoside Rh2: un promettente trattamento adiuvante per la leucemia promielocitica acuta

Introduzione
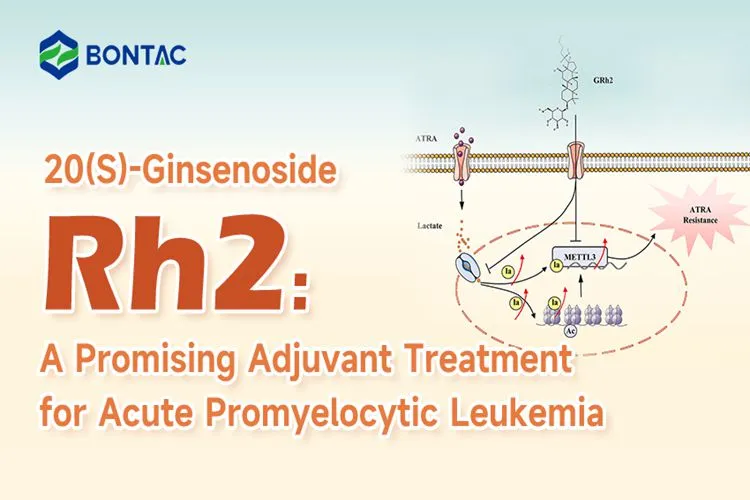
La leucemia promielocitica acuta (APL), il tipo M3 di leucemia mieloide acuta (AML), si basa tipicamente sull'acido retinoico all-trans (ATRA) come trattamento primario. Mentre i pazienti con APL trattati con ATRA mostrano un alto tasso di remissione completa del midollo osseo, la resistenza all'ATRA ne limita gravemente l'efficacia e contribuisce a una prognosi infausta. Recenti ricerche sottolineano il potenziale del 20(S)-ginsenoside Rh2 (GRh2) come inibitore METTL3 modificato per lattilazione per migliorare la resistenza all'ATRA nell'APL, fornendo una nuova direzione per lo sviluppo di nuovi farmaci per l'APL.
Informazioni su APL
L'APL, che costituisce il 10-15% di tutti i casi di LMA, è caratterizzata da un'anomala proliferazione dei promielociti, con complicanze associate come la disfunzione del midollo osseo e l'anemia. Negli anni '60 e '70, l'APL è un'emergenza medica con un alto tasso di mortalità e la morte correlata all'API è spesso attribuita a sanguinamento dovuto a disturbi della coagulazione. Con l'invenzione e l'evoluzione di nuovi farmaci, la prognosi dei pazienti con APL è stata notevolmente migliorata. Il tasso di sopravvivenza a 10 anni per i pazienti con APL oggi è stimato in circa l'80-90%. L'agente che induce la differenziazione, come l'ATRA, è una parte essenziale per il trattamento dell'APL. Le cellule staminali leucemiche (LSC) e le cellule APL resistenti all'ATRA contribuiscono principalmente alla recidiva della leucemia post-remissione. Affrontare questi problemi residui è di grande importanza nel perseguimento di migliori risultati terapeutici.
L'associazione tra METTL3 e resistenza all'ATRA nell'APL
METTL3 è un promettente bersaglio terapeutico per l'APL resistente all'ATRA. L'upregolazione di METTL3, che è guidata da modifiche della lattilazione, promuove la resistenza all'ATRA nell'APL, come indicato dall'aumento del numero di cellule leucemiche CD45+ e di cellule Giemsa positive nel gruppo METTL3-OE.
L'impatto soppressivo di GRh2 sulla resistenza all'ATRA nell'APL
In vitro, GRh2 aumenta i livelli di acetilazione degli istoni e inibisce notevolmente il livello di lattilazione nelle cellule APL resistenti agli ATRA e promuove l'apoptosi delle LSC resistenti agli ATRA, agendo come inibitore della lattilazione degli istoni. Oltre a reprimere l'attività enzimatica di METTL3, GRh2 inibisce in modo dose-dipendente i livelli di espressione di METTL3 e MEETL3 e della sua proteina di lettura a valle YTHDF2, YTHDF1 e YTHDC1 nelle cellule APL resistenti all'ATRA. L'analisi del docking molecolare mostra che GRh2 può legarsi direttamente con METTL3.
In vivo, GRh2 sopprime l'espressione di METTL3, il peso e il volume del tumore, ma migliora la sensibilità alla terapia di differenziazione ATRA nei topi con tumori xenotrapianto APL resistenti ad ATRA. Inoltre, il trattamento con GRh2 aumenta notevolmente la sopravvivenza dei topi xenotrapiantati APL resistenti all'ATRA.
Conclusione
Meccanicamente, GRh2 può ridurre la resistenza ATRA nell'APL reprimendo METTL3 guidato dalla lattilazione. Un'ulteriore esplorazione di questa interazione potrebbe portare allo sviluppo di strategie di trattamento più efficaci e personalizzate per i pazienti con APL, migliorando in ultima analisi la loro prognosi e la qualità della vita.
Riferimento
Cheng S, Chen L, Ying J, et al. 20(S)-ginsenoside Rh2 migliora la resistenza all'ATRA nell'APL modulando METTL3 guidato dalla lattilazione. J Ginseng Res. 2024; 48(3):298-309. DOI:10.1016/j.jgr.2023.12.003
BONTAC Ginsenosidi
BONTACsi dedica alla ricerca e sviluppo, alla produzione e alla vendita di materie prime per coenzima e prodotti naturali dal 2012, con fabbriche di proprietà, oltre 170 brevetti globali e un forte team di ricerca e sviluppo. BONTAC ha una ricca esperienza di ricerca e sviluppo e una tecnologia avanzata nella biosintesi diginsenosidi rari Rh2/Rg3, con materie prime pure, tasso di conversione più elevato e contenuto più elevato (fino al 99%). In BONTAC è disponibile un servizio completo per soluzioni di prodotto personalizzate. ConBonzimatecnologia di sintesi enzimatica, sia gli isomeri di tipo S che quelli di tipo R possono essere sintetizzati con precisione, con un'attività più forte e un'azione di targeting precisa. I nostri prodotti sono sottoposti a rigorosa autoispezione da parte di terzi, che vale la pena di essere affidabile.
Disconoscimento
Questo articolo si basa sul riferimento nella rivista accademica. Le informazioni pertinenti sono fornite solo a scopo di condivisione e apprendimento e non rappresentano alcuna consulenza medica. In caso di violazione, si prega di contattare l'autore per la cancellazione. Le opinioni espresse in questo articolo non rappresentano la posizione di BONTAC. In nessun caso BONTAC sarà responsabile per eventuali reclami, danni, perdite, spese o costi derivanti direttamente o indirettamente dall'affidamento dell'utente sulle informazioni e sul materiale di questo sito web.
